UPUTA O LIJEKU
Budosan 2 mg rektalna pjena
budezonid
Pažljivo pročitajte cijelu uputu prije nego počnete primjenjivati lijek jer sadrži Vama važne podatke.
- Sačuvajte ovu uputu. Možda ćete je trebati ponovno pročitati.
- Ako imate dodatnih pitanja, obratite se Vašem liječniku ili ljekarniku.
- Ovaj je lijek propisan samo Vama. Nemojte ga davati drugima. Može im naškoditi,, čak i ako su njihovi znakovi bolesti jednaki Vašima.
- Ako primijetite bilo koju nuspojavu, potrebno je obavijestiti Vašeg liječnika ili ljekarnika. To uključuje i svaku moguću nuspojavu koja nije navedena u ovoj uputi. Pogledajte dio 4.
Što se nalazi u ovoj uputi:
- Što je Budosan rektalna pjena i za što se koristi?
- Što morate znati prije nego počnete primjenjivati Budosan rektalnu pjenu?
- Kako primjenjivati Budosan rektalnu pjenu?
- Moguće nuspojave
- Kako čuvati Budosan rektalnu pjenu?
- Sadržaj pakiranja i druge informacije
- ŠTO JE BUDOSAN REKTALNA PJENA I ZA ŠTO SE KORISTI?
Budosan rektalna pjena je lijek za crijeva i sadržava djelatnu tvar budezonid, lokalno djelujući kortikosteroid za liječenje kroničnih upalnih bolesti crijeva.
Budosan ektalna pjena koristi se za liječenje akutnih epizoda kronične upale rektuma i zadnjeg dijela debelog crijeva (ulcerozni kolitis).
- ŠTO MORATE ZNATI PRIJE NEGO POČNETE KORISTITI BUDOSAN REKTALNU PJENU?
Nemojte primjenjivati Budosan rektalnu pjenu:
- ako ste alergični na budezonid ili neki drugi sastojak ovog lijeka (naveden u dijelu 6.),
- ako imate tešku bolest jetre (cirozu jetre).
Upozorenja i mjere opreza
Obratite se Vašem liječniku prije nego primijenite Budosan rektalnu pjenu ako imate:
- tuberkulozu
- visok krvni tlak
- dijabetes, ili ako je dijabetes dijagnosticiran u Vašoj obitelji
- krhke kosti (osteoporozu)
- čir želuca ili početnog dijela tankog crijeva (peptički ulkus)
- povišen tlak u očima (glaukom) ili probleme s očima, kao što je zamućenje leće (katarakta) ili ako je glaukom dijagnosticiran u Vašoj obitelji
- ozbiljne probleme s jetrom.
Mogu se javiti nuspojave tipične za preparate kortizona koje mogu zahvatiti sve dijelove tijela, osobito kada primjenjujete Budosan 2 mg rektalnu pjenu u visokim dozama i kroz dulje vrijeme (vidjeti dio 4. Moguće nuspojave).
Dodatne mjere opreza za vrijeme liječenja Budosan rektalnom pjenom:
- Obavijestite Vašeg liječnika ako imate neku infekciju. Simptomi nekih infekcija mogu biti atipični ili slabije izraženi.
- Držite se podalje od osoba koje imaju vodene kozice ili herpes zoster (crveni osip kože u struku) ako ih nikada niste imali. Mogli bi ozbiljno djelovati na Vaše zdravlje. Ako dođete u kontakt s vodenim kozicama ili herpes zosterom, odmah se javite Vašem liječniku.
- Obavijestite Vašeg liječnika ako do sada niste imali ospice.
- Ako znate da se trebate cijepiti, molimo prvo razgovarajte s Vašim liječnikom.
- Ako znate da se spremate na operaciju, molimo obavijestite Vašeg liječnika da primjenjujete Budosan 2 mg rektalnu pjenu.
- Ako ste bili liječeni snažnijim preparatom kortizona prije početka liječenja Budosan 2 mg rektalnom pjenom, Vaši simptomi se mogu ponovno pojaviti kod promjene lijeka. Ako se to dogodi, obratite se Vašem liječniku.
- Obratite se liječniku u slučaju zamućenog vida ili drugih poremećaja vida.
Drugi lijekovi i Budosan rektalna pjena
Obavijestite Vašeg liječnika ili ljekarnika ako primjenjujete, nedavno ste primijenili ili biste mogli primijeniti bilo koje druge lijekove. Osobito:
- srčane glikozide kao što je digoksin (lijekovi koji se primjenjuju za liječenje srčanih stanja)
- diuretike (za uklanjanje suvišne tekućine iz tijela)
- ketokonazol ili itrakonazol (za liječenje gljivičnih infekcija)
- antibiotike koji se primjenjuju za liječenje infekcija (kao što je klaritromicin)
- karbamazepin (primjenjuje se u liječenju epilepsije)
- rifampicin (za liječenje tuberkuloze)
- estrogene ili oralne kontraceptive
Neki lijekovi mogu povećati učinke lijeka Budosan rektalne pjene i ako uzimate takve lijekove (uključujući neke lijekove za HIV: ritonavir, kobicistat), vaš liječnik će vas možda htjeti pažljivo pratiti.
Budosan rektalna pjena može utjecati na rezultate ispitivanja koje provodi Vaš liječnik ili bolnica. Obavijestite Vašeg liječnika da primjenjujete Budosan rektalnu pjenu prije provođenja bilo kakvih ispitivanja.
Budosan rektalna pjena s hranom i pićem
Dok primjenjujete ovaj lijek ne smijete piti sok od grejpa jer on može promijeniti djelovanje lijeka.
Trudnoća i dojenje
Ako ste trudni ili dojite, mislite da biste mogli biti trudni ili planirate trudnoću, obratite se Vašem liječniku za savjet prije primjene ovog lijeka.
Smijete primijeniti Budosan rektalnu pjenu za vrijeme trudnoće samo ako Vam je liječnik to propisao.
Budezonid u malim količinama prelazi u mlijeko. Ako dojite, Budosan rektalnu pjenu smijete primijeniti samo ako Vam je liječnik to propisao.
Upravljanje vozilima i strojevima
Nije za očekivati da će Budosan rektalna pjena utjecati na Vašu sposobnost vožnje ili rada sa strojevima.
Budosan rektalna pjena sadrži cetilni alkohol i propilenglikol
Ovaj lijek sadrži cetilni alkohol i propilenglikol koji mogu uzrokovati lokalnu nadraženost kože (npr. kontaktni dermatitis).
- KAKO KORISTITI BUDOSAN REKTALNU PJENU
Uvijek primijenite ovaj lijek točno onako kako Vam je rekao Vaš liječnik. Provjerite s Vašim liječnikom ili ljekarnikom ako niste sigurni.
Doziranje:
Odrasli:
Jednom dnevno primijeniti 1 potisnu dozu (koja sadržava 2 mg budezonida).
Djeca i adolescenti:
Budosan 2 mg pjenu za rektum ne bi trebalo primijeniti u djece i adolescenata zbog malo iskustva u ovoj dobnoj skupini.
Način primjene:
Ovaj lijek se smije primjenjivati samo rektalno (uvođenje u zadnje crijevo).
Nije namijenjen uzimanju kroz usta i ne smije se progutati.
Budosan 2 mg rektalna pjena može se primijeniti ujutro ili navečer.
Najbolji učinak se postiže ako se crijeva isprazne prije primjene Budosan 2 mg rektalne pjene.

Aplikator (pomoć pri uvođenju) nalazi se u posebnoj spojnici. Držite ju čvrsto i naglim
pokretom izvucite aplikator.
Priprema za primjenu pjene:

Pazite da je Budosan 2 mg rektalna pjena prije primjene sobne temperature. Pričvrstite aplikator na mlaznicu limenke. Snažno tresite limenku 10 do 15 sekundi kako bi se sadržaj promiješao.

Prije prve primjene, ispod glave pumpe izvući sigurnosni dio (plastični jezičac) ispod glave pumpe.

Zakrenite glavu pumpe s vrha limenke sve dok polukružni utor nije u ravnini s mlaznicom. Limenka je tek tada spremna za uporabu.
Primjena pjene:

Postavite kažiprst na glavu pumpe i okrenite limenku naopako. Molimo obratite pažnju da će limenka funkcionirati pravilno samo onda kada glavu pumpe držite što je više moguće okomito prema dolje.

Uvedite aplikator toliko duboko u rektum koliko možete. Najbolje je da pritom stavite jednu nogu na stolicu. Kako bi primijenili jednu dozu Budosan 2 mg rektalne pjene, jednom pritisnite glavu pumpe do kraja i držite ju oko 2 sekunde. Tada ju vrlo polako otpuštajte. Pjena je sada dospjela u crijevo. Pričekajte 10 do 15 sekundi prije nego što izvučete aplikator iz rektuma, kako bi se aplikator potpuno ispraznio. Pjena se još uvijek širi i inače bi neiskorištena istjecala iz aplikatora.

Nakon primjene pjene izvucite aplikator, te ga u priloženoj plastičnoj vrećici uklonite putem kućnog otpada. Za svaku primjenu koristite novi aplikator. Kako bi između primjena spriječili slučajan gubitak pjene iz limenke, zakrenite glavu pumpe tako da je utor na suprotnoj strani od mlaznice.
Trajanje primjene
Trajanje primjene određuje nadležni liječnik. Akutne epizode obično se smiruju nakon 6 do 8 tjedana. Nakon tog vremena Budosan 2 mg rektalna pjena ne bi se više trebala koristiti.
Molimo obratite se Vašem liječniku ako imate dojam da je djelovanje Budosan 2 mg rektalne pjene prejako ili preslabo.
Ako primijenite više Budosan 2 mg rektalne pjene nego što ste trebali
Trajanje primjene određuje nadležni liječnik. Akutne epizode obično se smiruju nakon 6 do 8 tjedana. Nakon tog vremena Budosan 2 mg rektalna pjena ne bi se više trebala koristiti.
Molimo obratite se Vašem liječniku ako imate dojam da je djelovanje Budosan 2 mg rektalne pjene prejako ili preslabo.
Ako ste zaboravili primijeniti Budosan 2 mg rektalnu pjenu
Ako zaboravite jednu dozu, samo dalje nastavite Vaše liječenje propisanom dozom. Nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljenu dozu.
Ako prestanete koristiti Budosan 2 mg rektalnu pjenu
Javite se Vašem liječniku ako želite prekinuti ili ranije završiti Vaše liječenje. Važno je da ne prestanete primijenjivati lijek naglo jer biste mogli oboljeti. Nastavite primijenjivati Vaš lijek sve dok Vam liječnik ne kaže da prestanete, čak i ako ste se počeli osjećati bolje.
Ako imate bilo kakvih pitanja u vezi s primjenom ovog lijeka, obratite se Vašem liječniku ili ljekarniku.
- MOGUĆE NUSPOJAVE
Kao i svi lijekovi, ovaj lijek može uzrokovati nuspojave iako se one neće pojaviti kod svakoga.
Ako primijetite bilo koji od sljedećih simptoma nakon primjene ovog lijeka, odmah se obratite Vašem liječniku:
- infekcija – javlja se često (može se javiti u manje od 1 na 10 osoba)
- glavobolja – javlja se često (može se javiti u manje od 1 na 10 osoba)
- promjene ponašanja, na primjer:
- depresija, razdražljivost, euforija – javljaju se često (mogu se javiti u manje od 1 na 10 osoba)
- nemir s povećanom tjelesnom aktivnošću, tjeskoba – javljaju se manje često (mogu se javiti kod do 1 na 100 osoba)
- agresivnost – javlja se rijetko (može se javiti u manje od 1 na 1000 osoba).
Prijavljene su također sljedeće nuspojave:
Često: mogu se javiti kod do 1 na 10 osoba
- pečenje ili bol u rektumu
- Cushingov sindrom – okruglo lice, porast težine, smanjena podnošljivost glukoze, visok šećer u krvi (šećerna bolest), povišeni krvni tlak, zadržavanje tekućine u tijelu (npr. otekline nogu), pojačano izlučivanje kalija (hipokalijemija), neredovite menstruacije u žena, neželjene dlake na tijelu u žena, impotencija, abnormalni laboratorijski nalazi (smanjena funkcija ili neaktivnost nadbubrežne žlijezde), crvene pruge na koži (strije), akne
- probavne smetnje, nadraženi želudac (dispepsija)
- bol u mišićima i zglobovima, slabost mišića, trzanje mišića
- krhke kosti (osteoporoza)
- osip zbog reakcije preosjetljivosti, crvene mrlje zbog krvarenja u koži, sporije cijeljenje rana, lokalne reakcije na koži kao što je kontaktni dermatitis
Manje često: mogu se javiti kod do 1 na 100 osoba
- povećan apetit
- promjene krvne slike (povišene vrijednosti sedimentacije eritrocita, povišen broj bijelih krvnih zrnaca)
- mučnina, bolovi u trbuhu, vjetrovi, trnci u abdomenu ili utrnulost abdomena, analna fisura, usni čirevi, česta potreba za pražnjenjem crijeva, rektalno krvarenje
- čirevi želuca ili tankog crijeva
- promjene u parametrima funkcije jetre
- promjene u funkciji gušterače, promjene hormona nadbubrežne žlijezde
- infekcije urinarnog trakta
- vrtoglavica, poremećaji osjeta mirisa
- nesanica, pojačano znojenje, slabost
Rijetko: mogu se javiti kod do 1na 1000 osoba
- zamućen vid, povišen očni tlak (glaukom), očna mrena (katarakta)
- upala gušterače (pankreatitis)
- oštećenje kostiju zbog slabe cirkulacije krvi što izaziva bol u kukovima, koljenima ili ramenima (avaskularna nekroza)
- stvaranje (nastanak) modrica
Vrlo rijetko: mogu se javiti kod do 1 na 10 000 osoba
- usporen rast u djece
- konstipacija
- povišen tlak u mozgu, moguće s povišenim tlakom u očima (oticanje optičkog diska) u adolescenata
- povećan rizik od zgrušavanja krvi, upala krvnih žila (povezano s prestankom primjene kortizona nakon dugotrajnog liječenja)
- umor, osjećaj opće slabosti
Ove nuspojave su tipične za steroidne lijekove i najveći dio njih može se očekivati i kod liječenja drugim steroidima. Mogu se javiti ovisno o dozi, o trajanju liječenja, o tome da li ste se liječili ili se liječite drugim preparatima kortizona te o Vašoj individualnoj osjetljivosti.
Neke od ovih neželjenih nuspojava prijavljene su tek nakon dugoročnog korištenja oralnog budezonida.
U pravilu je rizik od nuspojava kod Budosan 2 mg rektalne pjene manji nego kod pripravaka kortizona sa sistemskim djelovanjem (utječe na cijelo tijelo) zbog njegovog lokalnog djelovanja.
Ako ste bili liječeni snažnijim preparatom kortizona prije početka liječenja Budosan 2 mg rektalnom pjenom, Vaši simptomi se mogu ponovno pojaviti kod promjene lijeka.
Prijavljivanje nuspojava
Agencija za lijekove i medicinske proizvode (HALMED)
Internetska stranica: www.halmed.hr ili potražite HALMED aplikaciju putem Google Play ili Apple App Store trgovine
Prijavljivanjem nuspojava možete pridonijeti u procjeni sigurnosti ovog lijeka.
- Kako čuvati Budosan 2 mg rektalnu pjenu?
Ovaj lijek čuvajte izvan pogleda i dohvata djece.
Ovaj lijek se ne smije upotrijebiti nakon isteka roka valjanosti navedenog na kutiji i dnu spremnika. Rok valjanosti odnosi se na zadnji dan navedenog mjeseca.
Čuvajte na temperaturi ispod 25°C. Ne odlagati u hladnjak ili zamrzavati!
Spremnik je pod tlakom i sadržava 6,5% mase zapaljivog potisnog plina. Držati podalje od izvora vatre, uključujući cigarete. Čuvati zaštićeno od direktne sunčeve svjetlosti. Spremnik, čak i nakon uporabe, ne otvarati nasilno, bušiti ili spaljivati. Ne koristiti u blizini plamena ili usijanih predmeta.
Sadržaj se mora upotrijebiti unutar 4 tjedna nakon otvaranja spremnika.
Nikada nemojte nikakve lijekove bacati u otpadne vode ili kućni otpad. Pitajte Vašeg ljekarnika kako baciti lijekove koje više ne koristite. Ove će mjere pomoći u očuvanju okoliša.
- Sadržaj pakiranja i druge informacije
Što Budosan 2 mg rektalna pjena sadrži?
- Djelatna tvar je budezonid. Svaka potisna doza sadrži 2 mg budezonida.
- Pomoćne tvari su: propilenglikol; voda, pročišćena; emulgirajući vosak; makrogolstearileter; cetilni alkohol; citratna kiselina hidrat; dinatrijev edetat te propan; n-butan i izobutan kao potisni plinovi.
Kako Budosan 2 mg rektalna pjena izgleda i sadržaj pakiranja?
Budosan 2 mg rektalna pjena je bijela do bijelo-siva, kremasta čvrsta pjena.
Budosan 2 mg rektalna pjena dostupna je u pakiranjima od:
- 1 spremnik s 14 potisnih doza, 14 aplikatora i 14 plastičnih vrećica za higijensko odlaganje aplikatora, u kutiji
- 2 spremnika sa po 14 potisnih doza, 28 aplikatora i 28 plastičnih vrećica za higijensko odlaganje aplikatora, u kutiji
Jedan spremnik Budosan 2 mg rektalne pjene sadrži najmanje 14 potisnih doza (svaka potisna doza sadrži 1,2 g pjene za rektum).
Nositelj odobrenja za stavljanje lijeka u promet i proizvođač
Dr. Falk Pharma GmbH
Leinenweberstr. 5
79108 Freiburg, Njemačka
tel: +49 761 1514 0
e-mail: zentrale@drfalkpharma.de
Predstavnik nositelja odobrenja za Republiku Hrvatsku
WÜRTH d.o.o.
Lopašićeva 6
10000 Zagreb
tel: +385 1 4650358
e-mail: info@wurth.hr
Način i mjesto izdavanja lijeka
Lijek se izdaje na recept, u ljekarni.
Ova uputa je posljednji put revidirana 02. kolovoza 2021.
SAŽETAK OPISA SVOJSTAVA LIJEKA
- NAZIV LIJEKA
Budosan 2 mg rektalna pjena
- KVALITATIVNI I KVANTITATIVNI SASTAV
1 potisna doza sadrži 2 mg budezonida.
Pomoćne tvari s poznatim učinkom
Jedna potisna doza Budosan 2mg rektalne pjene sadrži 600,3 mg propilenglikola, 8,4 mg cetilnog alkohola i 15,1 mg cetostearilnog alkohola (komponenta emulgirajućeg voska).
Za cjeloviti popis pomoćnih tvari vidjeti dio 6.1.
- FARMACEUTSKI OBLIK
Rektalna pjena
Izgled: bijela do bijelosiva, kremasta čvrsta pjena
- KLINIČKI PODACI
4.1 Terapijske indikacije
Liječenje akutnih epizoda ulceroznog kolitisa koji je ograničen na rektum i sigmoidni kolon.
4.2 Doziranje i način primjene
Doziranje
Odrasli
1 potisna doza 2 mg budezonida dnevno.
Pedijatrijska populacija
Budosan 2 mg rektalnu pjenu ne bi trebalo primijeniti u djece i adolescenata zbog malo iskustva o primjeni u ovoj dobnoj skupini.
Način primjene
Za rektalnu primjenu
Budosan 2 mg rektalna pjena može se primijeniti ujutro ili navečer.
Budosan 2 mg rektalna pjena treba prije primjene biti sobne temperature.
Prije uvoĎenja aplikatora u rektum (toliko duboko koliko je bolesniku podnošljivo), na spremnik je potrebno postaviti aplikator i snažno ga protresti (oko 15 sekundi). Doziranje lijeka bit će točnije ukoliko se glava pumpe drži što je moguće više okomito prema dolje. Za primjenu jedne doze Budosan 2 mg rektalne pjene potrebno je do kraja pritisnuti glavu pumpe i polako ju otpuštati. Aplikator je nakon potiskivanja doze, a prije izvlačenja iz rektuma, potrebno u istom položaju držati 10 do 15 sekundi.
Najbolji učinak se postiže ako se crijeva isprazne prije primjene Budosan 2 mg rektalne pjene.
Trajanje liječenja
Trajanje primjene određuje nadležni liječnik. Akutne epizode ulceroznog kolitisa obično se smiruju nakon 6 do 8 tjedana, te se nakon tog vremena Budosan 2 mg rektalna pjena ne bi više trebala koristiti.
4.3 Kontraindikacije
Budosan 2 mg rektalna pjena ne smije se primijeniti u bolesnika s:
- preosjetljivošću na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1,
- cirozom jetre.
4.4 Posebna upozorenja i mjere opreza pri uporabi
Liječenje Budosan 2 mg rektalnom pjenom rezultira nižim sistemskim razinama steroida nego uobičajena terapija oralnim glukokortikosteroidima sa sistemski djelujućim kortikoidima. Prelazak s druge terapije glukokortikosteroidima može stoga dovesti do ponovnog pojavljivanja ili povratka simptoma povezanih s promjenom sistemskih razina steroida.
Oprez je potreban u bolesnika s tuberkulozom, hipertenzijom, diabetes mellitusom, osteoporozom, peptičkim ulkusom, glaukomom, kataraktom, dijabetesom u obiteljskoj anamnezi, glaukomom u obiteljskoj anamnezi ili nekim drugim stanjima u kojima glukokortikosteroidi mogu imati neželjene učinke.
Pojaviti se mogu sistemski učinci glukokortikosteroida, osobito kada je lijek propisan u visokim dozama i kroz dulje vrijeme. Ovi učinci mogu uključivati Cushingov sindrom, adrenalnu supresiju, usporen rast, smanjenu gustoću minerala kostiju, kataraktu, glaukom i širok raspon psihijatrijskih nuspojava ili onih koji utječu na ponašanje (vidjeti dio 4.8).
Infekcije
Supresija upalnog odgovora i imunološke funkcije povećava sklonost infekcijama i njihovu ozbiljnost. U obzir se pažljivo mora uzeti rizik od pogoršanja infekcija bakterijama, gljivicama, amebama i virusima za vrijeme liječenja glukokortikosteroidima. Klinička izraženost često može biti atipična, a teške infekcije, kao što su sepsa i tuberkuloza, mogu biti maskirane i tako dostići uznapredovali stadij prije nego što su prepoznate.
Vodene kozice
Posebna pažnja mora se obratiti na infekciju vodenim kozicama, budući da ova obično blaga bolest može biti smrtonosna u imunosuprimiranih bolesnika. Bolesnike koji ovu bolest još nisu preboljeli treba savjetovati da izbjegavaju bliski kontakt s osobama koje imaju vodene kozice ili herpes zoster, te da odmah potraže hitnu liječničku pomoć ako su izloženi. Ako je bolesnik dijete, roditelju se mora dati gore navedeni savjet. Pasivna imunizacija imunoglobulinom varicella zoster (VZIG) potrebna je za sve izložene neimunizirane bolesnike koji primaju sistemske glukokortiksteroide ili su ih primili u zadnja 3 mjeseca; potrebno ju je primijeniti unutar 10 dana od izloženosti vodenim kozicama. Ako je dijagnoza vodenih kozica potvrđena, bolest zahtijeva pažnju specijalista i hitno liječenje. Primjena glukokortikosteroida se ne smije prekinuti, a u slučaju potrebe dozu je moguće povećati.
Ospice
Bolesnici kompromitiranog imuniteta koji dođu u kontakt s ospicama trebali bi, kada god je moguće, primiti normalni imunoglobulin što je ranije moguće nakon izloženosti.
Cjepiva
Živa cjepiva se ne smiju primjenjivati u osoba koje kronično uzimaju glukokortikosteroide. Odgovor protutijela na druga cjepiva može biti umanjen.
Bolesnici s oštećenjem funkcije jetre
Temeljem iskustva s bolesnicima koji imaju kasni stadij primarne bilijarne ciroze (PBC) uz već razvijenu jetrenu cirozu, očekuje se povećana sistemska raspoloživost budezonida u svih bolesnika s teškim oštećenjem funkcije jetre.
Međutim, budezonid je u dnevnim oralnim dozama od 9 mg bio siguran i dobro podnošljiv za bolesnike s bolestima jetre bez ciroze jetre. Nema dokaza za potrebom posebne preporuke doziranja lijeka za bolesnike s necirotičnim bolestima jetre ili blagim oštećenjem funkcije jetre.
Poremećaj vida
Pri sustavnoj i topikalnoj uporabi kortikosteroida moguća je pojava poremećaja vida. Ako bolesnik ima simptome kao što su zamućen vid ili neke druge poremećaje vida, treba razmotriti potrebu da ga se uputi oftalmologu radi procjene mogućih uzroka, koji mogu uključivati kataraktu, glaukom ili rijetke bolesti kao što je centralna serozna korioretinopatija (CSCR) koja je zabilježena nakon sustavne i topikalne uporabe kortikosteroida.
Ostalo
Glukokortikosteroidi mogu uzrokovati supresiju hipotalamo-pituitarno-adrenalne osovine (HPA) te smanjiti odgovor na stres. Dodatno liječenje sistemskim glukokortikosteroidima se preporučuje u bolesnika s planiranom operacijom ili u drugim stresnim situacijama.
Treba izbjegavati istodobno liječenje ketokonazolom ili drugim inhibitorima CYP3A4 (vidjeti dio 4.5).
Ovaj lijek sadrži 600,3 mg propilenglikola u jednoj potisnoj dozi Budosan rektalne pjene. Propilenglikol može uzrokovati iritaciju kože.
Cetilni alkohol i cetostearilni alkohol uzrokuju lokalnu nadraženost kože (npr. kontaktni dermatitis).
4.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Farmakodinamičke interakcije
Srčani glikozidi
Djelovanje glikozida može biti pojačano zbog nedostatka kalija.
Saluretici
Izlučivanje kalija može biti pojačano.
Farmakokinetičke interakcije
Citokrom P450
Očekuje se da će istodobna primjena inhibitora CYP3A, uključujući lijekove koji sadrže kobicistat, povećati rizik od sistemskih nuspojava. Kombinaciju treba izbjegavati, osim kada korist nadmašuje povećani rizik od sistemskih nuspojava kortikosteroida, a u tom slučaju je bolesnike potrebno pratiti radi otkrivanja sistemskih nuspojava kortikosteroida.
Ketokonazol 200 mg jednom dnevno kroz usta povisio je koncentracije budezonida (3 mg u pojedinačnoj dozi) u plazmi za oko 6 puta za vrijeme istodobne primjene. Kada se ketokonazol primijenio 12 sati nakon budezonida, koncentracije su bile povišene za oko 3 puta. Budući da nema dovoljno podataka za preporuku doze, kombinaciju bi trebalo izbjegavati.
Ostali potentni inhibitori CYP3A4, kao što su ritonavir, itrakonazol, klaritromicin i sok od grejpa također mogu uzrokovati znatno povišenje koncentracija budezonida u plazmi. Stoga treba izbjegavati istodobno uzimanje budezonida.
Tvari ili lijekovi koji induciraju CYP3A4, kao što su karbamazepin i rifampicin, mogu umanjiti sistemsku, ali i lokalnu izloženost budezonida u sluznici crijeva. Tada može biti potrebna prilagodba doze.
Tvari ili lijekovi koji se metaboliziraju putem CYP3A4 mogu biti kompetitivni budezonidu. Ako je afinitet kompetitivne tvari za CYP3A4 snažniji, tada to može dovesti do povišene koncentracije budezonida u plazmi, ili – ako se budezonid snažnije veže na CYP3A4 – može doći do povišene razine kompetitivne tvari u plazmi, kada će možda biti potrebna prilagodba/smanjenje doze tog lijeka.
U žena, koje su istodobno primale estrogene ili oralne kontraceptive, prijavljene su povišene razine u plazmi i pojačano djelovanje glukokortikosteroida, no ovo nije primijećeno uz oralne kombinirane kontraceptive niske doze.
Iz razloga što liječenjem budezonidom može doći do supresije funkcije nadbubrežnih žlijezda, ACTH stimulacijski test koji se koristi za dijagnozu zatajenja hipofize može prikazati neispravne rezultate (niske vrijednosti).
4.6 Plodnost, trudnoća i dojenje
Trudnoća
Primjenu u trudnoći treba izbjegavati, osim ako ne postoje uvjerljivi razlozi za liječenje Budosan 2 mg rektalnom pjenom. Postoji malo podataka o ishodima trudnoće nakon oralne primjene budezonida u ljudi. Iako podaci o inhaliranom budezonidu u velikom broju izloženih trudnoća ne ukazuju na nuspojave, za očekivati je da će maksimalne koncentracije budezonida u plazmi biti više pri liječenju Budosan 2 mg rektalnom pjenom u usporedbi s inhaliranim budezonidom. Budezonid je, kao i drugi glukokortikosteroidi, na skotnim životinjama uzrokovao abnormalnosti u razvoju fetusa (vidjeti dio 5.3). Nije utvrđena važnost ovog učinka u ljudi.
Dojenje
Budezonid se izlučuje u majčino mlijeko (dostupni su podaci o izlučivanju nakon uporabe putem inhalacije). Za očekivati je međutim samo manje učinke na dojenče nakon uzimanja Budosana 2 mg rektalne pjene u terapijskom rasponu. Uzimajući u obzir koristi dojenja za dijete i korist liječenja za majku, mora se odlučiti hoće li se prekinuti dojenje ili će se prekinuti/suzdržati od liječenja budezonidom.
Plodnost
Nema podataka o učinku budezonida na plodnost u ljudi. U ispitivanjima na životinjama nije bilo utjecaja na plodnost nakon liječenja budezonidom (vidjeti dio 5.3) .
4.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Ispitivanja utjecaja na sposobnost upravljanja vozilima i rada na strojevima nisu provedena.
4.8 Nuspojave
Pri procjeni nuspojava korištene su slijedeće konvencije učestalosti:
vrlo često (≥ 1/10)
često (≥ 1/100 i < 1/10)
manje često (≥ 1/1000 i < 1/100)
rijetko (≥ 1/10 000 i < 1/1000)
vrlo rijetko (<1/10 000), nepoznato (ne može se procijeniti iz dostupnih podataka).
|
Klasifikacija organskih sustava
|
Učestalost prema konvenciji MedDRA
|
Nuspojave
|
|
Poremećaji metabolizma i prehrane
|
Često
|
Cushingov sindrom: okruglo lice („moon face“), centripetalni tip pretilosti, smanjena tolerancija glukoze, diabetes melitus, hipertenzija, zadržavanje natrija s nastankom edema, pojačano izlučivanje kalija, neaktivnost ili atrofija adrenalnog korteksa, crvene strije, steroidne akne, poremećaj izlučivanja spolnih hormona (npr. amenoreja, hirzutizam, impotencija)
|
|
Vrlo rijetko
|
Zaostajanje u rastu u djece
|
|
Poremećaji oka
|
Rijetko
|
Glaukom, katarakta, zamućen vid (vidjeti također dio 4.4.)
|
|
Poremećaji probavnog sustava
|
Često
|
Dispepsija
|
|
Manje često
|
Čir na dvanaesniku ili čir na želucu
|
|
Rijetko
|
Pankreatitis
|
|
Vrlo rijetko
|
Konstipacija
|
|
Poremećaji imunološkog sustava
|
Često
|
Povećan rizik od infekcija
|
|
Poremećaji mišićno-koštanog sustava i vezivnog tkiva
|
Često
|
Bol u mišićima i zglobovima, slabost i trzanje u mišićima, osteoporoza
|
|
Rijetko
|
Avaskularna nekroza
|
|
Poremećaji živčanog sustava
|
Često
|
Glavobolja
|
|
Vrlo rijetko
|
Pseudotumor cerebri uključujući papiloedem u adolescenata
|
|
Psihijatrijski poremećaji
|
Često
|
Depresija, razdražljivost, euforija
|
|
Manje često
|
Psihomotorička hiperaktivnost, tjeskoba
|
|
Rijetko
|
Agresivnost
|
|
Poremećaji kože i potkožnog tkiva
|
Često
|
Alergijski egzantem, petehije, odgođeno cijeljenje rana, kontaktni dermatitis
|
|
Rijetko
|
Ekhimoza
|
|
Krvožilni poremećaji
|
Vrlo rijetko
|
Povećan rizik od tromboze, vaskulitis (sindrom sustezanja nakon dugotrajnog liječenja)
|
|
Opći poremećaji i reakcije na mjestu primjene
|
Često
|
Pečenje i bol u rektumu
|
|
Vrlo rijetko
|
Umor, malaksalost
|
Sljedeće nuspojave dodatno su izviještene u kliničkim studijama s Budosan 2 mg rektalnom pjenom (učestalost: manje često): povećan apetit, povećana razina sedimentacije eritrocita, leukocitoza, mučnina, bol u trbuhu, nadutost, parestezije u području trbuha, analna fisura, aftozni stomatitis, čest nagon za pražnjenjem crijeva, rektalno krvarenje, povišene transaminaze (GOT, GPT), povišeni parametri kolestaza (GGT, AP), povišene amilaze, promjene u razini kortizola, infekcije urinarnog trakta, vrtoglavica, poremećaji u osjetu mirisa, nesanica, pojačano znojenje, astenija, povećanje tjelesne težine.
Najveći broj nuspojava navedenih u ovom sažetku opisa svojstava lijeka mogu se očekivati i pri liječenju drugim glukokortikosteroidima.
Povremeno se mogu javiti nuspojave tipične za sistemske glukokortikosteroide. Ove su nuspojave ovisne o dozi, trajanju liječenja, istodobnom ili prijašnjem liječenju drugim glukokortikosteroidima, te individualnoj osjetljivosti.
Neke od ovih neželjenih nuspojava prijavljene su tek nakon dugoročnog korištenja oralnog budezonida.
U pravilu je rizik od nuspojava kod Budosan 2 mg rektalne pjene manji nego kod uzimanja glukokortikosteroida sa sistemskim djelovanjem.
Egzacerbacija ili ponovna pojava ekstraintestinalnih manifestacija (osobito onih koje zahvaćaju kožu i zglobove) mogu se javiti kod prelaska bolesnika sa sistemski djelujućih glukokortikosteroida na lokalno djelujući budezonid.
Prijavljivanje sumnji na nuspojavu
Nakon dobivanja odobrenja lijeka, važno je prijavljivanje sumnji na njegove nuspojave. Time se omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih radnika traži se da prijave svaku sumnju na nuspojavu lijeka putem nacionalnog sustava prijave nuspojava: navedenog u Dodatku V.
4.9 Predoziranje
Do sada nema poznatih slučajeva predoziranja budezonidom.
- FARMAKOLOŠKA SVOJSTVA
5.1 Farmakodinamička svojstva
Farmakoterapijska skupina: Antidijaroici i pripravci s antiinflamatornim i antiinfektivnim djelovanjem, kortikosteroidi koji djeluju lokalno
ATK oznaka: A07EA06
Točan mehanizam djelovanja budezonida u liječenju ulceroznog kolitisa/proktosigmoiditisa nije još u potpunosti razjašnjen. Rezultati kliničko-farmakoloških i drugih kontroliranih kliničkih studija snažno ukazuju da se učinkovitost budezonida uglavnom temelji na njegovoj lokalnoj djelotvornosti u crijevu. Budezonid je glukokortikoid s jakim lokalnim protuupalnim djelovanjem.
U dozi od 2 mg rektalno primijenjenog budezonida, koja je klinički ekvivalentna sistemski djelujućim glukokortikoidima, budezonid gotovo da ne uzrokuje supresiju hipotalamo-pituitarno-adrenalne osovine.
Budosan 2 mg rektalna pjena u ispitivanoj dozi od 4 mg budezonida na dan gotovo da nema utjecaja na razinu kortizola u plazmi.
5.2 Farmakokinetička svojstva
Općeniti aspekti budezonida:
Apsorpcija
Sistemska raspoloživost budezonida nakon oralne primjene je oko 10%.
Distribucija
Budezonid ima veliki volumen distribucije (oko 3 l/kg). Vezanje na proteine plazme u prosjeku iznosi 85 – 90%.
Biotransformacija
Budezonid se intenzivno metabolizira u jetri (oko 90%) na metabolite slabog glukokortikoidnog djelovanja. U usporedbi s budezonidom, glukokortikoidno djelovanje glavnih metabolita 6ß-hidroksibudezonida i 16α-hidroksiprednizolona – koji se tvore putem CYP3A – je manje od 1%.
Eliminacija
Prosječni terminalni polu-život eliminacije nakon oralne primjene iznosi oko 3 – 4 sata. Srednji klirens budezonida iznosi oko 10 l/min.
Posebne skupine bolesnika (bolesnici s oštećenjem funkcije jetre)
Ovisno o vrsti i ozbiljnosti oštećenja funkcije jetre, metabolizam budezonida putem CYP3A može u ovih bolesnika biti smanjen.
Specifični aspekti Budosan 2 mg rektalne pjene:
Apsorpcija:
Područja ispod krivulje koncentracija/vrijeme su nakon rektalne primjene nešto viša nego nakon oralne primjene (historijska kontrola). Vršne razine se nakon primjene Budosan 2 mg rektalne pjene postižu u prosjeku nakon 2 – 3 sata.
Kumulacija nakon ponovljenih primjena može se isključiti.
Raspodjela:
Scintigrafsko ispitivanje s Budosan 2 mg rektalnom pjenom, označenom tehnecijem, u bolesnika s ulceroznim kolitisom pokazalo je raspodjelu pjene kroz cijeli sigmoid.
5.3 Neklinički podaci o sigurnosti primjene
Nakon ponovljene oralne primjene budezonida (u dozama kao i kod ljudi), u štakora je primijećeno smanjenje broja leukocita (osobito trombocita) i regresija timusa. Postojale su i naznake atrofijom uzrokovane adrenalne neaktivnosti. U žlijezdama dojke je primijećena pojačana proliferacija mliječnih kanala i sekretorna aktivnost. U jednoj dugotrajnoj studiji (104 tjedna), u ženki štakora je bio smanjen broj hematokrita, hemoglobina i eritrocita. U skupinama s istom dozom postojala je tendencija povećanog broja neutrofila i smanjenih vrijednosti limfocita, eozinofila i normocita. Značajno smanjenje broja limfocita bilo je prisutno samo kod muških životinja (imunosupresivni učinak), kao i lagano povišena alkalna fosfataza.
U pasa su ustanovljene smanjene vrijednosti „packed cells“ volumena, povišene koncentracije alkalne fosfataze i alanin-aminotransferaze, adrenalna atrofija i atrofija limfatičnog sustava, povećana masna masa u miokardu, te povišeni sadržaj glikogena u jetri (povećanje jetre).
Mutagenost:
Budezonid nije pokazao mutagene učinke niti u jednom od brojnih in vitro i in vivo testova.
Kancerogenost:
Mužjaci štakora tretirani budezonidom do 104 tjedna razvili su lagano povećanu incidenciju bazofilnih nakupina u jetri, u usporedbi s kontrolnim životinjama. Incidencija primarnih hepatocelularnih neoplazmi (0,025 i 0,05 mg/kg tjelesne težine/dan), astrocitoma (mužjaci štakora: 0,05 mg/kg tjelesne težine/dan) i tumora dojke (ženke štakora: 0,05 mg/kg tjelesne težine/dan) značajno je povećana u studiji kancerogenosti. Tumori jetre vjerojatno su nastali zbog anaboličkog učinka i povećanog metaboličkog opterećenja za jetru. Rezultati su pokazali klasni učinak u koji su vjerojatno uključeni receptori glukokortikoida.
Reproduktivna toksičnost:
U ispitivanjima na životinjama različitih vrsta, glukokortikoidi su inducirali teratogene učinke (rascjep nepca, skeletne malformacije).
Klinički značaj ovih svojstava do sada još nije razjašnjen. Budezonid je nakon supkutane primjene u glodavaca pokazao promjene već poznate za ostale glukokortikoide.
Ispitivanja na životinjama su također pokazala da primjena sintetskih glukokortikoida za vrijeme gestacije može dovesti do povećanog rizika od retardacije intrauterinog rasta i doprinijeti razvoju krvožilnih bolesti i/ili bolesti metabolizma u odraslih, kao i trajnim promjenama u gustoći receptora glukokortikoida, protoku neurotransmitera i ponašanju.
- FARMACEUTSKI PODACI
6.1 Popis pomoćnih tvari
Propilenglikol,
Voda, pročišćena,
Emulgirajući vosak,
Makrogolstearileter,
Cetilni alkohol,
Citratna kiselina hidrat,
Dinatrijev edetat,
Propelenti:
Propan,
N-butan,
Izobutan.
6.2 Inkompatibilnosti
Nije primjenjivo
6.3 Rok valjanosti
3 godine
Nakon prve primjene:
4 tjedna
6.4 Posebne mjere pri čuvanju lijeka
Čuvati na temperaturi do 25°C. Ne odlagati u hladnjak i ne zamrzavati.
Spremnik je pod tlakom i sadrži 6,5% mase zapaljivog propelenta. Držati podalje od izvora vatre, uključujući cigarete. Čuvati zaštićeno od direktne sunčeve svjetlosti. Spremnik, čak i nakon uporabe, ne otvarati nasilno, bušiti ili spaljivati. Ne koristiti u blizini plamena ili usijanih predmeta.
6.5 Vrsta i sadržaj spremnika
Aluminijski spremnik pod tlakom s odmjernim ventilom; 14 ili 28 aplikatora od PVC-a za primjenu pjene koji su obloženi bijelim vazelinom i tekućim parafinom; 14 ili 28 plastičnih vrećica za higijensko uklanjanje aplikatora.
Veličine pakiranja:
- 1 spremnik s 14 potisnih doza, 14 aplikatora i 14 plastičnih vrećica za higijensko odlaganje aplikatora, u kutiji
- 2 spremnika sa po 14 potisnih doza, 28 aplikatora i 28 plastičnih vrećica za higijensko odlaganje aplikatora, u kutiji
Jedan spremnik Budosan 2 mg rektalne pjene sadrži najmanje 14 potisnih doza (jedna potisna doza sadrži 1,2 g pjene za rektum).
6.6 Posebne mjere za zbrinjavanje
Nema posebnih zahtjeva.
7. NOSITELJ ODOBRENJA ZA STAVLJANJE LIJEKA U PROMET
Dr. Falk Pharma GmbH
Leinenweberstr. 5
79108 Freiburg, Njemačka
tel: +49 761 1514 0
e-mail: zentrale@drfalkpharma.de
8. BROJ(EVI) ODOBRENJA ZA STAVLJANJE LIJEKA U PROMET
- DATUM PRVOG ODOBRENJA /DATUM OBNOVE ODOBRENJA
Datum prvog odobrenja: 15. listopada 2012.
Datum posljednje obnove odobrenja: 27. ožujka 2018.
- DATUM REVIZIJE TEKSTA
17.11.2022.
Za liječenje akutnih epizoda ulceroznog kolitisa koji je ograničen na rektum i sigmoidni kolon, po preporuci specijalista internista ili pedijatra.

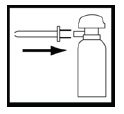 Pazite da je Budosan 2 mg rektalna pjena prije primjene sobne temperature. Pričvrstite aplikator na mlaznicu limenke. Snažno tresite limenku 10 do 15 sekundi kako bi se sadržaj promiješao.
Pazite da je Budosan 2 mg rektalna pjena prije primjene sobne temperature. Pričvrstite aplikator na mlaznicu limenke. Snažno tresite limenku 10 do 15 sekundi kako bi se sadržaj promiješao.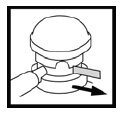 Prije prve primjene, ispod glave pumpe izvući sigurnosni dio (plastični jezičac) ispod glave pumpe.
Prije prve primjene, ispod glave pumpe izvući sigurnosni dio (plastični jezičac) ispod glave pumpe.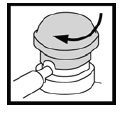 Zakrenite glavu pumpe s vrha limenke sve dok polukružni utor nije u ravnini s mlaznicom. Limenka je tek tada spremna za uporabu.
Zakrenite glavu pumpe s vrha limenke sve dok polukružni utor nije u ravnini s mlaznicom. Limenka je tek tada spremna za uporabu.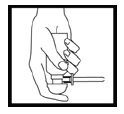 Postavite kažiprst na glavu pumpe i okrenite limenku naopako. Molimo obratite pažnju da će limenka funkcionirati pravilno samo onda kada glavu pumpe držite što je više moguće okomito prema dolje.
Postavite kažiprst na glavu pumpe i okrenite limenku naopako. Molimo obratite pažnju da će limenka funkcionirati pravilno samo onda kada glavu pumpe držite što je više moguće okomito prema dolje.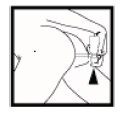 Uvedite aplikator toliko duboko u rektum koliko možete. Najbolje je da pritom stavite jednu nogu na stolicu. Kako bi primijenili jednu dozu Budosan 2 mg rektalne pjene, jednom pritisnite glavu pumpe do kraja i držite ju oko 2 sekunde. Tada ju vrlo polako otpuštajte. Pjena je sada dospjela u crijevo. Pričekajte 10 do 15 sekundi prije nego što izvučete aplikator iz rektuma, kako bi se aplikator potpuno ispraznio. Pjena se još uvijek širi i inače bi neiskorištena istjecala iz aplikatora.
Uvedite aplikator toliko duboko u rektum koliko možete. Najbolje je da pritom stavite jednu nogu na stolicu. Kako bi primijenili jednu dozu Budosan 2 mg rektalne pjene, jednom pritisnite glavu pumpe do kraja i držite ju oko 2 sekunde. Tada ju vrlo polako otpuštajte. Pjena je sada dospjela u crijevo. Pričekajte 10 do 15 sekundi prije nego što izvučete aplikator iz rektuma, kako bi se aplikator potpuno ispraznio. Pjena se još uvijek širi i inače bi neiskorištena istjecala iz aplikatora.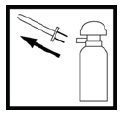 Nakon primjene pjene izvucite aplikator, te ga u priloženoj plastičnoj vrećici uklonite putem kućnog otpada. Za svaku primjenu koristite novi aplikator. Kako bi između primjena spriječili slučajan gubitak pjene iz limenke, zakrenite glavu pumpe tako da je utor na suprotnoj strani od mlaznice.
Nakon primjene pjene izvucite aplikator, te ga u priloženoj plastičnoj vrećici uklonite putem kućnog otpada. Za svaku primjenu koristite novi aplikator. Kako bi između primjena spriječili slučajan gubitak pjene iz limenke, zakrenite glavu pumpe tako da je utor na suprotnoj strani od mlaznice.